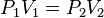Buscar este blog
miércoles, 24 de noviembre de 2010
martes, 16 de noviembre de 2010
Acidos y bases. PH
Ácidos y bases, son dos tipos de compuestos químicos que presentan características opuestas.
Los ácidos tienen un sabor agrio, colorean de rojo el tornasol (tinte rosa que se obtiene de determinados líquenes) y reaccionan con ciertos metales desprendiendo hidrógeno.
Las bases tienen sabor amargo, colorean el tornasol de azul y tienen tacto jabonoso. Cuando se combina una disolución acuosa de un ácido con otra de una base, tiene lugar una reacción de neutralización. Esta reacción en la que, generalmente, se forman agua y sal, es muy rápida. Así, el ácido sulfúrico y el hidróxido de sodio NaOH, producen agua y sulfato de sodio:
H2SO4 + 2NaOHð2H2O + Na2SO4
Mira el vídeo explicativo.
Interacción dipolo dipolo.
La interacción dipolo-dipolo (visto en el enlace puente de hidrógeno) consiste en la atracción electrostática entre el extremo positivo de una molécula polar y el negativo de otra.
Las fuerzas electrostáticas entre dos iones disminuyen de acuerdo con un factor 1/d2 a medida que aumenta su separación d. En cambio, las fuerzas dipolo dipolo varían según 1/d4 (d elevado a la cuarta potencia) y sólo son eficaces a distancias muy cortas.
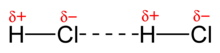
Definición extraída de Wikipedia.
Enlace de Hidrógeno.
 El enlace de Hidrógeno o Puente de Hidrógeno resulta de la formación de una fuerza dipolo-dipolo con un átomo de hidrógeno unido a un átomo de nitrógeno, oxígeno o flúor.
El enlace de Hidrógeno o Puente de Hidrógeno resulta de la formación de una fuerza dipolo-dipolo con un átomo de hidrógeno unido a un átomo de nitrógeno, oxígeno o flúor.Es la fuerza atractiva entre un átomo electronegativo y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo.
La energía de un enlace de hidrógeno (típicamente de 5 a 30 kJ/mol) es comparable a la de los enlaces covalentes débiles (155 kJ/mol), y un enlace covalente típico es sólo 20 veces más fuerte que un enlace de hidrógeno intermolecular. Es decir el enlace de hidrógeno es una fuerza fija muy fuerte, pero más débil que el enlace covalente o el enlace iónico.
Este tipo de enlace ocurre tanto en moléculas inorgánicas tales como el agua, y en moléculas orgánicas como el ADN.
jueves, 11 de noviembre de 2010
Diferencias entre modelo atómico de Bohr y el de Rutherford.
El modelo de Rutherford solo describe al atomo con un nucleo y entorno a él se encuentran girando los electrones en orbitas, algo similar a como los planetas lo hacen entorno al sol... De hecho a este modelo tambien se le llama el modelo del sistema solar.

El modelo de Bohr establece que los electrones entorno al nucleo se encuentran en niveles bien definidos de energia... y que si ganan energia suben d nivel y si pierden energia bajan de nivel.
 La diferencia fundamentala entre los dos modelos es que uno considera los niveles de energia y el otro no lo hace.
La diferencia fundamentala entre los dos modelos es que uno considera los niveles de energia y el otro no lo hace.

El modelo de Bohr establece que los electrones entorno al nucleo se encuentran en niveles bien definidos de energia... y que si ganan energia suben d nivel y si pierden energia bajan de nivel.

Modelo atómico de Bhor.
El modelo atómico de Bohr parte, conceptualmente, del modelo atómico de Rutherford y de las incipientes ideas sobre cuantización que habían surgido unos años antes con las investigaciones de Max Planck y Albert Einstein.
En 1913 Niels Bohr propuso que los electrones estaban separados de las partículas positivas y que el átomo semejaba un sistema solar donde las cargas negativas orbitaban alrededor del núcleo de carga positiva, el modelo atómico de Bohr quedó expuesto en sus postulados.
Postulados de Bohr:
1.- Los electrones giran alrededor del núcleo en orbitas fijas llamdos orbitales.
2.- Entre mayor sea el orbital mayor será el contenido de energía del electrón.
3.- Para que un electrón cambie de orbital necesita ganar o desprender energía.
4.- La energía ganada o perdida por el electrón es una cantidad fija llamada cuanto que significa salto.

En 1913 Niels Bohr propuso que los electrones estaban separados de las partículas positivas y que el átomo semejaba un sistema solar donde las cargas negativas orbitaban alrededor del núcleo de carga positiva, el modelo atómico de Bohr quedó expuesto en sus postulados.
Postulados de Bohr:
1.- Los electrones giran alrededor del núcleo en orbitas fijas llamdos orbitales.
2.- Entre mayor sea el orbital mayor será el contenido de energía del electrón.
3.- Para que un electrón cambie de orbital necesita ganar o desprender energía.
4.- La energía ganada o perdida por el electrón es una cantidad fija llamada cuanto que significa salto.

martes, 9 de noviembre de 2010
El experimento de Thomson.,
Thomson fue elegido Miembro de la Royal Society y galardonado con el Premio Nobel de Física por sus innumerables teorías y aportaciones sobre conductividad eléctrica en gases.
Pero fue por lo que se conoce como el tercer experimento de Thomson el más importante:


Pero fue por lo que se conoce como el tercer experimento de Thomson el más importante:

Según este esquema , que ilustra el tercer experimento, Thomson observó que el campo eléctrico desviaba los rayos catódicos (los rayos catódicos son corrientes de electrones que se mueven en el vacío) en sentido vertical hacia la placa positiva. Ello demostraba la carga eléctrica negativa inherente a estos rayos y la existencia de una masa y de la consiguiente inercia, que impedía que fueran absorbidos por la placa. Por tanto, debía existir una partícula elemental constituyente de los rayos catódicos, a la que se llamó electrón.
Thomson determinó el valor de la relación entre la carga e y la masa m del electrón, que hoy día se acepta como:
Thomson determinó el valor de la relación entre la carga e y la masa m del electrón, que hoy día se acepta como:

Más tarde Rutherford con otro experimento ajustó la teoría y descubrió con él que existían protones en el núcleo. El modelo atómico de Rutherford fue modificado por el modelo atómico de Bhor.
Modelo atómico de Thomson.,
El modelo de Thomson fue expuesta cien años después del modelo atómico de Dalton y es anterior y precursor al de Rutherford.
En dicho modelo, el átomo está compuesto por electrones, desconocido hasta la fecha, de carga negativa en un átomo positivo (el descubrimiento del núcleo tal y como lo conocemos ahora aun no se había realizado).

El átomo no deja de ser un sistema material que contiene una cierta cantidad de energía externa. Ésta provoca un cierto grado de atracción de los electrones contenidos en la estructura atómica.
Cómo se descubrió el electrón. Experimentos de Thomson.
En dicho modelo, el átomo está compuesto por electrones, desconocido hasta la fecha, de carga negativa en un átomo positivo (el descubrimiento del núcleo tal y como lo conocemos ahora aun no se había realizado).

El átomo no deja de ser un sistema material que contiene una cierta cantidad de energía externa. Ésta provoca un cierto grado de atracción de los electrones contenidos en la estructura atómica.
Cómo se descubrió el electrón. Experimentos de Thomson.
Modelo atómico de Rutherford.
Después del modelo atómico de Dalton y depués el de Thomson Ernest Rutherford, siguió complementando la teoria. Para Rutherford el átomo era un sistema planetario de electrones (descritos ya en a¡el sistema de Thomson) girando alrededor de un núcleo atómico pesado y con carga eléctrica positiva.
El módelo atómico de Rutherford puede resumirse de la siguiente manera:
El átomo posee un núcleo central pequeño, con carga eléctrica positiva, que contiene casi toda la masa del átomo.
Los electrones giran a grandes distancias alrededor del núcleo en órbitas circulares.
La suma de las cargas eléctricas negativas de los electrones debe ser igual a la carga positiva del núcleo, ya que el átomo es eléctricamente neutro.
Rutherford no solo dio una idea de cómo estaba organizado un átomo, sino que también calculó cuidadosamente su tamaño (un diámetro del orden de 10-10 m) y el de su núcleo (un diámetro del orden de 10-14m). El hecho de que el núcleo tenga un diámetro unas diez mil veces menor que el átomo supone una gran cantidad de espacio vacío en la organización atómica de la materia.
El módelo atómico de Rutherford puede resumirse de la siguiente manera:
El átomo posee un núcleo central pequeño, con carga eléctrica positiva, que contiene casi toda la masa del átomo.
Los electrones giran a grandes distancias alrededor del núcleo en órbitas circulares.
La suma de las cargas eléctricas negativas de los electrones debe ser igual a la carga positiva del núcleo, ya que el átomo es eléctricamente neutro.
Rutherford no solo dio una idea de cómo estaba organizado un átomo, sino que también calculó cuidadosamente su tamaño (un diámetro del orden de 10-10 m) y el de su núcleo (un diámetro del orden de 10-14m). El hecho de que el núcleo tenga un diámetro unas diez mil veces menor que el átomo supone una gran cantidad de espacio vacío en la organización atómica de la materia.
Modelo atómico de Dalton.
El modelo atómico de Dalton fue el primer modelo atómico con bases científicas de la historia, fue formulado en 1808 por John Dalton.
Dalton explicó su teoría formulando una serie de enunciados simples:
La materia está formada por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir.
Los átomos de un mismo elemento son iguales entre sí, tienen su propio peso y cualidades propias. Los átomos de los diferentes elementos tienen pesos diferentes.
Los átomos permanecen sin división, aún cuando se combinen en las reacciones químicas.
Los átomos, al combinarse para formar compuestos guardan relaciones simples.
Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
Los compuestos químicos se forman al unirse átomos de dos o más elementos distintos.
El modelo atómico de Dalton explicaba por qué las sustancias se combinaban químicamente entre sí sólo en ciertas proporciones.
Además el modelo aclaraba que aún existiendo una gran variedad de sustancias diferentes, estas podían ser explicadas en términos de una cantidad más bien pequeña de constituyentes elementales o elementos.
En esencia, el modelo explicaba la mayor parte de la química orgánica del siglo XIX, reduciendo una serie de hechos complejos a una teoría combinatoria realmente simple.
El siguiente modelo fue el Modelo atómico de Thomson
Dalton explicó su teoría formulando una serie de enunciados simples:
La materia está formada por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir.
Los átomos de un mismo elemento son iguales entre sí, tienen su propio peso y cualidades propias. Los átomos de los diferentes elementos tienen pesos diferentes.
Los átomos permanecen sin división, aún cuando se combinen en las reacciones químicas.
Los átomos, al combinarse para formar compuestos guardan relaciones simples.
Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
Los compuestos químicos se forman al unirse átomos de dos o más elementos distintos.
El modelo atómico de Dalton explicaba por qué las sustancias se combinaban químicamente entre sí sólo en ciertas proporciones.
Además el modelo aclaraba que aún existiendo una gran variedad de sustancias diferentes, estas podían ser explicadas en términos de una cantidad más bien pequeña de constituyentes elementales o elementos.
En esencia, el modelo explicaba la mayor parte de la química orgánica del siglo XIX, reduciendo una serie de hechos complejos a una teoría combinatoria realmente simple.
domingo, 7 de noviembre de 2010
Enlace químico y sus tipos.
Los átomos se unen entre sí formando enlaces químicos para tener la misma configuración electrónica que el gas noble más cercano y así ser más estable, o lo que es lo mismo, para que disminuya su energía.
Vamos a estudiar tres tipos de enlaces entre átomos: el enlace iónico, el enlace covalente y enlace metálico.
Vamos a estudiar tres tipos de enlaces entre átomos: el enlace iónico, el enlace covalente y enlace metálico.
Enlace metálico
El enlace metálico se produce cuando se combinan entre sí los elementos metálicos; es decir, elementos de electronegatividades bajas y que se diferencien poco.
Los metales forman unas redes metálicas compactas por lo que suelen tener altas densidades. Las redes suelen ser hexagonales y cúbicas.
1º Suelen ser sólidos a temperatura ambiente, excepto el mercurio, y sus puntos de fusión y ebullición varían notablemente.
Hay dos modelos que explican la formación del enlace metálico. El modelo de la nube de electrones y la teoría de bandas.
El modelo de la nube de electrones:
Los electrones no pertenencen a ningún átomo determinado. Los átomos metálicos ceden sus electrones de valencia a una "nube electrónica" que comprende todos los átomos del metal.
Esta teoría de bandas representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía).
Los metales forman unas redes metálicas compactas por lo que suelen tener altas densidades. Las redes suelen ser hexagonales y cúbicas.
Propiedades del enlace metálico.
1º Suelen ser sólidos a temperatura ambiente, excepto el mercurio, y sus puntos de fusión y ebullición varían notablemente.
2º Las conductividades térmicas y eléctricas son muy elevadas.
3º Presentan brillo metálico.
4º Son dúctiles y maleables.
5º Pueden emitir electrones cuando reciben energía en forma de calor.
El modelo de la nube de electrones:
Los electrones no pertenencen a ningún átomo determinado. Los átomos metálicos ceden sus electrones de valencia a una "nube electrónica" que comprende todos los átomos del metal.
Esta teoría de bandas representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía).
Enlace Iónico.
Este tipo de enlace se suele dar entre un metal y un no metal. El enlace iónico es una unión que resulta de la presencia de fuerza de atracción electrostática entre los iones de distinto signo. La fuerza electrostática es la fuerza que se produce entre polos de distinto signo (uno positivo y otro negativo).
1º Las sustancias iónicas se encuentran en la naturaleza formando redes cristalinas, por tanto son sólidas.
2º Su dureza es bastante grande, y tienen por lo tanto puntos de fusión y ebullición altos.
3º Son solubles en disolventes polares como el agua.
4º Cuando se tratan de sustancias disueltas tienen una conductividad alta.
Propiedades de los enlaces iónicos:
2º Su dureza es bastante grande, y tienen por lo tanto puntos de fusión y ebullición altos.
3º Son solubles en disolventes polares como el agua.
4º Cuando se tratan de sustancias disueltas tienen una conductividad alta.
Enlace Covalente.
El enlace covalente se forma por compartición de electrones entre los átomos que forman la molécula.
Cuando se unen dos átomos de elementos no metálicos que comparten pares de electrones para adquirir la configuración electrónica del gas noble más cercano.
Propiedades de los enlaces covalentes:
1º Los compuestos covalentes suelen presentarse en estado líquido o gaseoso aunque también pueden ser sólidos. Por lo tanto sus puntos de fusión y ebullición no son elevados.
2º La solubilidad de estos compuestos es elevada en disolventes polares, y nula su capacidad conductora.
3º Los sólidos covalentes macromoleculares, tienen altos puntos de fusión y ebullición, son duros, malos conductores y en general insolubles.
Cuando se unen dos átomos de elementos no metálicos que comparten pares de electrones para adquirir la configuración electrónica del gas noble más cercano.
Propiedades de los enlaces covalentes:
1º Los compuestos covalentes suelen presentarse en estado líquido o gaseoso aunque también pueden ser sólidos. Por lo tanto sus puntos de fusión y ebullición no son elevados.
2º La solubilidad de estos compuestos es elevada en disolventes polares, y nula su capacidad conductora.
3º Los sólidos covalentes macromoleculares, tienen altos puntos de fusión y ebullición, son duros, malos conductores y en general insolubles.
viernes, 5 de noviembre de 2010
Ejercicios y problemas resueltos de Gases Ideales. 2ª parte.
Estos problemas han sido extraídos de FisicaNet.com . Y han sido resueltos por el profesor Ricardo Santiago Netto. Allí puedes encontrar más ejercicios de Gases Ideales.
Problemas Resueltos de Gases Ideales2
Problemas Resueltos de Gases Ideales2
jueves, 4 de noviembre de 2010
Ley de Charles y Gay-Lussac
Esta ley relaciona el volumen y la temperatura de una cierta cantidad de gas ideal.
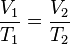
La ley de Charles dice así:
A una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que "temperatura" significa movimiento de las partículas. Así que, a mayor movimiento de las partículas (temperatura), mayor volumen del gas.
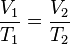
A una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que "temperatura" significa movimiento de las partículas. Así que, a mayor movimiento de las partículas (temperatura), mayor volumen del gas.
En este vídeo entenderéis claramente como reacciona un gas: cuando se le reduce la temperatura ( bajará el volumen) y si aumenta la temperatura ( aumentará el volumen).
Gases ideales.
Los gases que cumplen perfectamente las leyes de Boyle y de Charles y Gay-Lussac, reciben la denominación de GASES IDEALES.
La ecuación que describe normalmente la relación entre la presión, el volumen, la temperatura y la cantidad (en moles) de un gas ideal es:
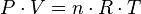
1ºUn gas ideal ejerce una presión continua sobre las paredes del recipiente que lo contiene, debido a los choques de las partículas con las paredes de éste.
2ºLos choques moleculares son perfectamente elásticos. No hay pérdida de energía cinética.
3ºNo se tienen en cuenta las interacciones de atracción y repulsión molecular.
La ecuación que describe normalmente la relación entre la presión, el volumen, la temperatura y la cantidad (en moles) de un gas ideal es:
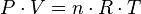
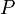 = Presión.
= Presión. = Volumen.
= Volumen.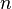 = Moles de Gas.
= Moles de Gas.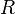 = Constante universal de los gases ideales.
= Constante universal de los gases ideales.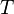 = Temperatura absoluta.
= Temperatura absoluta.
Los gases ideales, son gases hipotéticos, que no existen en la realidad y nos simplifican las operaciones.
Los gases reales que más se aproximan al comportamiento del gas ideal son los gases monoatómicos en condiciones de baja presión y alta temperatura.Algunas características de los gases ideales son:
1ºUn gas ideal ejerce una presión continua sobre las paredes del recipiente que lo contiene, debido a los choques de las partículas con las paredes de éste.
2ºLos choques moleculares son perfectamente elásticos. No hay pérdida de energía cinética.
3ºNo se tienen en cuenta las interacciones de atracción y repulsión molecular.
miércoles, 3 de noviembre de 2010
Cambios de estado progresivo y regresivo.

Cambios de estado progresivos: Son los cambios de estado cuando se aporta energía.
Estos son:
1º- De estado de sólido a líquido. Se denomina fusión.
Cada sólido se funde a una temperatura determinada, llamada comúnmente punto o temperatura de fusión.
Mientras dura el cambio de estado, la temperatura se mantiene constante. Osea, la energía transferida no aumenta la temperatura, simplemente debilita las fuerzas que mantienen unidas las moléculas del estado sólido.
El calor latente de fusión es la energía que se utiliza para fusionar 1kg de una sustancia sólida a estado líquido.
Q=mLfus.
2º- De líquido a gas. Vaporización.
Si en el proceso de vaporización pasa a estado gaseoso formando burbujas, se llama ebullición.
El cambio de estado se produce en la superficie libre del líquido.
El calor latente de vaporización es la energía necesaria para evaporar 1 Kg de una sustancia líquida a estado gaseoso.
Q=mLvap.
La temperatura necesaria para empezar a hervir un líquido se llama punto o temperatura de ebullición.
3º- De sólido a gas. Sublimación.
Consiste en el cambio de estado de la materia sólida al estadogaseoso sin pasar por el estado líquido.
Cambios de estado progresivos: en este tipo de cambios se desprende energía.
Estos son:
1º- De líquido a sólido.
Este proceso se llama solidificación o congelación. Y se produce en el punto o temperatura de congelación, que coincide con la temperatura de fusión del sólido.
2º- De gas a líquido.
Es el contrario a la evaporación, recibe el nombre de condensación. Por ejemplo el bao que se forma en el espejo.
3º- De gas a sólido.
Sublimación inversa o regresiva. Este proceso es muy poco frecuente.
martes, 2 de noviembre de 2010
Ajusta las reacciones método matemático.
Veamos los pasos para saber como ajustar reacciones químicas por el método matemático.
1º Asigna una letra a cada coeficiente estequiométrico. Conviene asignarlas por orden alfabético de izquierda a derecha.
2º Cogemos el primer elemento de la izquierda y planteamos la ecuación que representa el balance de átomos de dicho elemento:
Nº de átomos del elemento en la izquierda = Nº de átomos del elemento en la derecha
3º Continuando por la izquierda de la reacción química, planteamos otra ecuación para el siguiente elemento diferente. De esta forma tendremos el balance de átomos de todos los elementos diferentes que existen en la reacción química.
Siempre tendremos una ecuación menos que incógnitas. En algún caso podríamos obtener más ecuaciones pero si nos fijamos bien veremos que algunas son equivalentes.
4º Asignamos el valor 1 a la letra (incógnita) que queramos.
Resolvemos el resto de las ecuaciones.
5º Si en los resultados tenemos decimales o fracciones, debemos multiplicar todas las incógnitas por un mismo número de tal forma que desaparezcan
1º Asigna una letra a cada coeficiente estequiométrico. Conviene asignarlas por orden alfabético de izquierda a derecha.
2º Cogemos el primer elemento de la izquierda y planteamos la ecuación que representa el balance de átomos de dicho elemento:
Nº de átomos del elemento en la izquierda = Nº de átomos del elemento en la derecha
3º Continuando por la izquierda de la reacción química, planteamos otra ecuación para el siguiente elemento diferente. De esta forma tendremos el balance de átomos de todos los elementos diferentes que existen en la reacción química.
Siempre tendremos una ecuación menos que incógnitas. En algún caso podríamos obtener más ecuaciones pero si nos fijamos bien veremos que algunas son equivalentes.
4º Asignamos el valor 1 a la letra (incógnita) que queramos.
Resolvemos el resto de las ecuaciones.
5º Si en los resultados tenemos decimales o fracciones, debemos multiplicar todas las incógnitas por un mismo número de tal forma que desaparezcan
lunes, 1 de noviembre de 2010
Fórmula empírica y fórmula molecular.
Fórmula empírica.
La fórmula empírica de un compuesto es aquella que indica la relación más sencilla en la que están combinados los átomos de cada uno de los elementos.
Fórmula molecular.
La fórmula molecular expresa la relación existente entre los números de los diferentes átomos que forman parte de la molécula real de un compuesto.
Para calcular la fórmula molecular hay que calcular antes la fórmula empírica, a partir de la composición centesimal, el procedimiento es el siguiente:
1º Se calcula la cantidad de sustancia, en mol, de cada uno de los elementos dividiendo los porcentajes entre la masa atómica de cada elemento.
2º Si los coeficientes no son cifras enteras, se buscan otros enteros equivalentes dividiendo lo anteriores entre los más pequeños de todos, y si aun así no salen cifras exactas, se multiplican por el más pequeño. Se trata de encontrar una relación de números enteros entre los átomos que forman el compuesto.
Ejemplo:
Si la fórmula empírica es AB2
La fórmula molecular será (AB2)n
n= masa molar/ masa molar empírica.
La fórmula empírica de un compuesto es aquella que indica la relación más sencilla en la que están combinados los átomos de cada uno de los elementos.
Fórmula molecular.
La fórmula molecular expresa la relación existente entre los números de los diferentes átomos que forman parte de la molécula real de un compuesto.
Para calcular la fórmula molecular hay que calcular antes la fórmula empírica, a partir de la composición centesimal, el procedimiento es el siguiente:
1º Se calcula la cantidad de sustancia, en mol, de cada uno de los elementos dividiendo los porcentajes entre la masa atómica de cada elemento.
2º Si los coeficientes no son cifras enteras, se buscan otros enteros equivalentes dividiendo lo anteriores entre los más pequeños de todos, y si aun así no salen cifras exactas, se multiplican por el más pequeño. Se trata de encontrar una relación de números enteros entre los átomos que forman el compuesto.
Ejemplo:
Si la fórmula empírica es AB2
La fórmula molecular será (AB2)n
n= masa molar/ masa molar empírica.
Composición centesimal.
Cuando se conoce la fórmula de un compuesto, su composición química se expresa como el porcentaje en peso de cada uno de los elementos que la componen. La composición centesimal indica el porcentaje en masa, de cada elemento que forma parte de un compuesto.
Para calcular la composición centesimal de cada elemento, se aplica la siguiente expresión:

En donde ni indica el número de átomos del elemento i considerado y PMi la masa atómica de dicho elemento.
Ejemplo:
Queremos calcular el porcentaje de oxígeno presente en el ácido nítrico. Las masas moleculares son:
Hidrógeno = 1,008 uma.
Nitrógeno = 14,01 uma.
Oxígeno = 16,00 uma.
Peso molecular del ácido nítrico: uma.
uma.
Lo mismo puede repetirse para cada elemento.
VER FÓRMULA EMPÍRICA Y FÓRMULA MOLECULAR.
Para calcular la composición centesimal de cada elemento, se aplica la siguiente expresión:

En donde ni indica el número de átomos del elemento i considerado y PMi la masa atómica de dicho elemento.
Ejemplo:
Queremos calcular el porcentaje de oxígeno presente en el ácido nítrico. Las masas moleculares son:
Hidrógeno = 1,008 uma.
Nitrógeno = 14,01 uma.
Oxígeno = 16,00 uma.
Peso molecular del ácido nítrico:
 uma.
uma.La fórmula del ácido nítrico es HNO3, así sabemos que una molécula de ácido nítrico contiene un átomo de hidrógeno, uno de nitrógeno y tres de oxígeno. Aplicamos la fórmula anterior para el oxígeno.


Lo mismo puede repetirse para cada elemento.
VER FÓRMULA EMPÍRICA Y FÓRMULA MOLECULAR.
Suscribirse a:
Entradas (Atom)
FORMAS DE REPRESENTAR MOLÉCULAS ORGÁNICAS.
En la química del carbono, es fácil encontrar diversos compuestos diferentes con la misma fórmula molecular. Para diferenciarlos, debemos s...

-
En un átomo, los electrones están girando alrededor del núcleo formando capas. En cada una de ellas, la energía que posee el electrón es dis...
-
La Estructura o diagrama de Lewis es una representación gráfica que muestra los enlaces entre los átomos de una molécula y los pares de elec...
-
Cambios de estado progresivos : Son los cambios de estado cuando se aporta energía. Estos son: 1º- De estado de sólido a líquido . Se deno...