Buscar este blog
miércoles, 21 de diciembre de 2011
Teoría de la colisión de Lewis.
viernes, 9 de diciembre de 2011
¿Qué son los isótopos?

Número atómico y número másico.

martes, 15 de noviembre de 2011
Estructura de zig zag de las cadenas carbonatadas.

La presencia de átomos de carbono con enlaces dobles hace que dicho ángulo sea próximo a 120º, con estructura plana e impidiendo el giro o rotación sobre el eje C=C. Es el caso de los alquenos o los ácidos grasos insaturados.
La presencia de átomos de carbono con enlaces triples C≡C hace que dicho ángulo sea próximo a 180º, con geometría lineal y tramos rectos en la molécula, como en el caso de los alquinos.
Por cierto, ¿Qué es una cadena carbonatada? Una cadena carbonada es el esqueleto de la práctica totalidad de los compuestos orgánicos y está formada por un conjunto de varios átomos de carbono, unidos entre sí mediante enlaces covalentes carbono-carbono y a la que se unen o agregan otros átomos como hidrógeno, oxígeno o nitrógeno, formando variadas estructuras, lo que origina infinidad de compuestos diferentes.
Información extraída de Wikipedia.
Formación de enlaces sencillos, dobles y triples.



martes, 1 de noviembre de 2011
Configuraciones electrónicas. Bases y criterios.

lunes, 17 de octubre de 2011
Niveles energéticos atómicos
A su vez, cada nivel tiene sus electrones repartidos en distintos subniveles, que pueden ser de cuatro tipos: s, p, d, f.

domingo, 9 de octubre de 2011
Estructura y diagrama de Lewis.
 Los pasos para dibujar el diagrama de Lewis son:
Los pasos para dibujar el diagrama de Lewis son:1. Determinar el número total de electrones de valencia:
- En una molécula neutra, es la suma de los electrones de valencia de los átomos que la forman.
- En un anión, hay que añadir el número de electrones correspondientes a la carga del ión.
- En un catión, hay que restar el número de electrones correspondiente a la carga del ión.
2. Colocar los átomos en sus posiciones relativas:
- En algunos casos sólo hay una ordenación posible.
- En otros es necesario recurrir a información experimental para decidir entre dos o más ordenaciones posibles. En este sentido, el átomo central suele ser el menos electronegativo.
3. Dibujar una línea que representa un enlace sencillo conteniendo dos electrones entre átomos unidos.
4. Distribuir los electrones restantes (1) como pares de electrones de no enlace en los átomos exteriores, de tal manera que cada átomo tenga ocho electrones, (el hidrógeno sólo dos), si es posible.
Si aún queda algún electrón, éste debe ser colocado en el átomo central.
Estos electrones (1) se calculan restando al número total de electrones de valencia dos electrones por cada enlace de los dibujados en la regla 3.
5. Si el átomo central está rodeado por menos de ocho electrones, hay que desplazar el número suficiente de pares de electrones de no enlace de los átomos exteriores, (a excepción de los halógenos), colocándolos entre los átomos enlazados y transformándolos en pares de electrones de enlace con objeto de que el átomo central pasa a estar rodeado de ocho electrones.
6. Asignación de cargas formales.
La carga formal de un átomo en una molécula se calcula:
Carga formal = nº electrones de valencia del átomo – [mitad del nº de electrones compartidos + nº de electrones no compartidos]
miércoles, 28 de septiembre de 2011
Energía de un proceso químico.

martes, 27 de septiembre de 2011
Ley de Hess y ecuaciones termoquímica.
 La Ley de Hess dice: “si una serie de reactivos (por ej. A y B) reaccionan para dar una serie de productos (por ej. C y D), la cantidad de calor involucrado (liberado o absorbido), es siempre la misma, independientemente de si la reacción se lleva a cabo en una, dos o más etapas; siempre y cuando, las condiciones de presión y temperatura de las diferentes etapas sean las mismas”.
La Ley de Hess dice: “si una serie de reactivos (por ej. A y B) reaccionan para dar una serie de productos (por ej. C y D), la cantidad de calor involucrado (liberado o absorbido), es siempre la misma, independientemente de si la reacción se lleva a cabo en una, dos o más etapas; siempre y cuando, las condiciones de presión y temperatura de las diferentes etapas sean las mismas”.O sea: en toda reacción química hay ruptura y/o formación de nuevos enlaces químicos y para que haya esa ruptura y/o formación, se requiere energía, algunas veces, y otras se desprende la energía sobrante.
Reacciones de combustión.

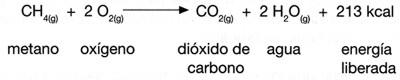
Los procesos de combustión y de oxidación tienen algo en común: la unión de una sustancia con el oxígeno. La única diferencia es la velocidad con que el proceso tiene lugar. Así, cuando el proceso de unión con el oxígeno es lo bastante lento como para que el calor desprendido durante el mismo se disipe en el ambiente sin calentar apreciablemente el cuerpo, se habla de oxidación. Si el proceso es rápido y va acompañado de un gran aumento de temperatura y en ocasiones de emisión de luz (llama), recibe el nombre de combustión.
lunes, 19 de septiembre de 2011
Espectros atómicos de absorción y de emisión.
Por tanto:
Espectro de absorción, radiación electromagnética absorbida por un átomo o molécula.
Espectro de emisión, radiación electromagnética emitida por un átomo en estado gaseoso.
Los espectros de absorción y de emisión resultan ser el negativo uno del otro. Esto quiere decir, que sabiendo los espectros de absorción podemos saber los de emisión y viceversa.
Puesto que el espectro, tanto de emisión como de absorción, es característico de cada elemento, podemos identificar con un simple análisis cada uno de los elementos de la tabla periódica.

Otro ejemplo: ¿Cómo crees que saben los astrónomos de qué se compone una galaxia a millones de años luz? Pues según la luz que emiten. El análisis detallado del espectro de emisión o de absorción de las estrellas, planetas y del medio interestelar permite identificar su composición química.
martes, 6 de septiembre de 2011
Partículas subatómicas. Tubos de descarga de gases.
 A partir del descubrimiento de los rayos catódicos J.J. Thomson llegó a la conclusión de que las partículas de los rayos catódicos debían de ser partículas constituyentes fundamentales de toda la materia.
A partir del descubrimiento de los rayos catódicos J.J. Thomson llegó a la conclusión de que las partículas de los rayos catódicos debían de ser partículas constituyentes fundamentales de toda la materia.jueves, 18 de agosto de 2011
Diagrama de Lewis.
2. Alrededor del átomo central se sitúan los demás (ligandos) de la forma más simétrica posible. En los oxácidos, generalmente el H se une al O. (En CO y NO, C y N son centrales).
6. Calcular la carga formal de cada átomo comenzando por el central. La carga formal es la carga hipotética que tiene cada átomo en la estructura de Lewis y se obtiene por diferencia entre los electrones de valencia del átomo libre y los asignados en la estructura a dicho átomo, es decir:
qf= nº e-valencia – (nº e-no enlazantes + nº enlaces)
desplazando un par no enlazante del ligando negativo al átomo central, lo que cancela un par de cargas formales, una negativa y otra positiva.
lunes, 1 de agosto de 2011
Radiación electromagnética: parámetros característicos.

Ciclo: Se denomina ciclo a cada patrón repetitivo de una onda.
Período: Es el tiempo que tarda la onda en completar un ciclo.
Frecuencia: Número de ciclos que completa la onda en un intervalo de tiempo. Si dicho intervalo es de un segundo, la unidad de frecuencia es el Hertz (Hz). Otras unidades de frecuencias muy utilizadas (en otros ámbitos) son las "revoluciones por minuto" (RPM) y los "radianes por segundo" (rad/s).
El período y la frecuencia están relacionados de la siguiente manera:
Amplitud: Es la medida de la magnitud de la máxima perturbación del medio producida por la onda.
Longitud: La longitud de una onda viene determinada por la distancia entre los puntos inicial y final de un ciclo (por ejemplo, entre un valle de la onda y el siguiente). Habitualmente se denota con la letra griega lambda.
Un factor importante a tener en cuenta es que el tamaño y diseño de las antenas está fuertemente influenciado por la longitud de onda. Por ejemplo, una antena dipolo sencilla debe tener una longitud lambda/2 para que sintonice de manera óptima las ondas de longitud lambda.
Los conceptos anteriores están representados en la siguiente figura tomada de la Wikipedia:
Velocidad: Las ondas se desplazan a una velocidad que depende de la naturaleza de la onda y del medio por el cual se mueven. En el caso de la luz, por ejemplo, la velocidad en el vacío se denota "c" y vale 299.792.458 m/s (aproximadamente 3.10^8 m/s).
Los conceptos de velocidad, longitud y frecuencia están interrelacionados. Para el caso de las ondas electromagnéticas (de las cuales la luz es un ejemplo), la relación es:
Fase: La fase de una onda relaciona la posición de una característica específica del ciclo (como por ejemplo un pico), con la posición de la misma característica en otra onda. Puede medirse en unidades de tiempo, distancia, fracción de la longitud de onda o (más comúnmente) como un ángulo.
Ahora puedes ver esta presentación para entender mejor las ondas y sus características.
miércoles, 27 de julio de 2011
Hidrocarburos aromáticos. Estructura del Benceno.
átomo de hidrógeno del núcleo bencénico por radicales alquílicos, o bien por condensación del núcleo bencénico. Ejemplo:

Nomenclatura (Con radicales de menos de cuatro carbonos):
Con un radical: Cuando hay un único sustituyente sobre el anillo bencénico, el nombre de aquel se antepone a la palabra benceno. Ejemplos:

estos con los números (1,2), (1,3) ó (1,4), ó los prefijos orto- (o-), meta- (m-) o para- (p-), respectivamente. Si los radicales son distintos se nombran por orden alfabético, y si son iguales, mediante los prefijos di-, tri-… Ejemplos:

Ejemplo:


El radical del benceno se denomina fenilo. Ejemplos:
Con cadenas lineales de 4 ó más carbonos el benceno se nombra como radical (fenil). Ejemplos:

Recordemos, que siempre y cuando el benceno actúe como radical, es decir, no tenga
más sustituyentes, prevalece el nombre de la cadena lineal si tiene 4 carbonos o más, en caso contrario se nombra como radical del benceno
martes, 12 de julio de 2011
SISTEMA PERIÓDICO Y FAMILIAS O GRUPOS.

Grupo 2. Metales alcalinotérreos. Berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra).
Grupo 13. Familia del boro o boroideos. Boro (B), aluminio (Al), galio (Ga), indio (In) y talio (Tl).
Grupo 14. Familia del carbono o carbonoideos. Carbono (C), silicio (Si), germanio (Ge), estaño (Sn) y plomo (Pb).
Grupo 15. Familia del nitrógeno o nitrogenoideos. Nitrógeno (N), fósforo (P), arsénico (As), antimonio (Sb) y bismuto (Bi).
Grupo 16. Familia del oxígeno o anfígenos. Oxígeno (O), azufre (S), selenio (Se), teluro (Te) y polonio (Po).
Grupo 17. Halógenos. Flúor (F), cloro (Cl), bromo (Br), yodo (I) y astato (At).
Grupo 18. Gases nobles. Helio (He), neón (Ne), argón (Ar), criptón (Kr), xenón (Xe) y radón (Rn).
Del 3 al 12. Elementos de transición. Algunos ejemplos: cromo (Cr), hierro (Fe), níquel (Ni), cobre (Cu), cinc (Zn), plata (Ag), platino (Pt), oro (Au) y mercurio (Hg).
Un «problema» sin solución, aunque no tiene especial relevancia, es la posición del hidrógeno (H). Hay químicos que lo consideran dentro del grupo 1, metales alcalinos. Otros dicen que podría situarse en el grupo 17, con los
jueves, 23 de junio de 2011
Hipótesis de Planck.
 Max Karl Ernest Ludwig Planck fue un físico alemán considerado como el fundador de la teoría cuántica.
Max Karl Ernest Ludwig Planck fue un físico alemán considerado como el fundador de la teoría cuántica.En 1889, descubrió una constante fundamental, la denominada Constante de Planck, usada para calcular la energía de un fotón. Planck establece que la energía se radia en unidades pequeñas denominadas cuantos. La ley de Planck relaciona que la energía de cada cuanto es igual a la frecuencia de la radiación multiplicada por la Constante de Planck. Un año después descubrió la ley de radiación del calor, denominada Ley de Planck, que explica el espectro de emisión de un cuerpo negro. Esta ley se convirtió en una de las bases de la teoría cuántica, que emergió unos años más tarde con la colaboración de Albert Einstein y Niels Böhr.
Lo que postuló Planck al introducir su ley es que la única manera de obtener una fórmula experimentalmente correcta exigía la novedosa y atrevida suposición de que dicho intercambio de energía debía suceder de una manera discontinua, es decir, a través de la emisión y absorción de cantidades discretas de energía, que hoy denominamos “quantums” de radiación.
 RESUMIENDO:
RESUMIENDO:Según Planck, la energía emitida o captada por un cuerpo en forma de radiación electromagnética es siempre un múltiplo de la constante h, llamada posteriormente constante de Planck por la frecuencia v de la radiación.
e =nhv
h=6,62 10-34 J·s, constante de Planck
v=frecuencia de la radiación
A hv le llamó cuanto de energía. Que un cuanto sea más energético que otro dependerá de su frecuencia.
martes, 24 de mayo de 2011
Características del carbono y su combinación.
El carbono es el elemento número 6 de la tabla periódica (Z=6 y A=12) y el primer elemento del Grupo IV. Su estructura electrónica es 1s2 2s2 2p2.
El átomo de carbono tiene 4 electrones en la última capa. Esto hace que pueda unirse a otros átomos mediante cuatro enlaces covalentes.
Número atómico 6
Valencia 2,+4,-4
Configuración electrónica 1s22s22p2
Masa atómica (g/mol) 12,01115
Densidad (g/ml) 2,26
Punto de fusión (ºC) 3727
2º Características por su importancia:
Al poder combinar de varias formas, el carbono es un elemento ideal para elaborar los complejos sistemas orgánicos como nuestras células o las hojas de las plantas. Siendo el número de combinación entre átomos de carbonos y otros diferentes es casi infinito.
Con el oxígeno forma dos compuestos gaseosos importantes: monóxido de carbono (CO), y dióxido de carbono (CO2).
LA COMBINACIÓN DEL CARBONO.
El carbono presenta una importante capacidad de combinación con otros átomos ya que puede formar hasta cuatro enlaces con otros átomos.
 La diversidad de los productos químicos orgánicos se debe a la infinidad de opciones que brinda el carbono para enlazarse con otros átomos. Los químicos orgánicos más simples, llamados hidrocarburos, contienen sólo carbono y átomos de hidrógeno; el hidrocarburo más simple (llamado metano) contiene un solo átomo de carbono enlazado a cuatro átomos de hidrógeno
La diversidad de los productos químicos orgánicos se debe a la infinidad de opciones que brinda el carbono para enlazarse con otros átomos. Los químicos orgánicos más simples, llamados hidrocarburos, contienen sólo carbono y átomos de hidrógeno; el hidrocarburo más simple (llamado metano) contiene un solo átomo de carbono enlazado a cuatro átomos de hidrógenoPero el carbono también puede enlazarse con otros átomos de carbono adicionalmente al hidrógeno tal como se ilustra en el siguiente dibujo de la molécula etano

Fuerzas intermoleculares.
*En términos relativos, si se da el valor 1 a la fuerza de unión de Van der Waals:
V. der Waals............1
P de Hidrógeno.......10
Enlace covalente.... 100
Las fuerzas de atracción explican la cohesión de las moléculas en los estados liquido y sólido de la materia, y se llaman fuerzas de largo alcance o Fuerzas de Van der Waals en honor al físico holandés Johannes van der Waals. Estas fuerzas son las responsables de muchos fenómenos físicos y químicos como la adhesión, rozamiento, difusión, tensión superficial y la viscosidad.
Entre las diferentes fuerzas de orden intermoleculares que mantienen unidos los átomos dentro de la molécula y ayudan a mantener la estabilidad de las moléculas individuales, las más conocidas son las siguientes:
1º- ENLACE O PUENTE DE HIDRÓGENO.
2º- FUERZAS DE VAN DER WAALS.
2.1º- DIPOLO-DIPOLO. Una atracción dipolo-dipolo es una interacción no covalente entre dos moléculas polares. Las moléculas que son dipolos se atraen entre sí cuando la región positiva de una está cerca de la región negativa de la otra. Podríamos decir que es similar al enlace ionico pero más débil.
 Son interacciones que ocurren a nivel de catión-anión, entre distintas moléculas cargadas, y que por lo mismo tenderán a formar una unión electrostática entre los extremos de cargas opuestas debido a la atracción entre ellas
Son interacciones que ocurren a nivel de catión-anión, entre distintas moléculas cargadas, y que por lo mismo tenderán a formar una unión electrostática entre los extremos de cargas opuestas debido a la atracción entre ellasLas fuerzas de London se presentan en todas las sustancias moleculares. Son el resultado de la atracción entre los extremos positivo y negativo de dipolos inducidos en moléculas adyacentes.En general, cuantos más electrones haya en una molécula más fácilmente podrá polarizarse. Así, las moléculas más grandes con muchos electrones son relativamente polarizables. En contraste, las moléculas más pequeñas son menos polarizables porque tienen menos electrones
Regla del Octeto.
Estas propiedades dependerán por tanto del tipo de enlace (covalente, ionico, metálico, y enlaces intermoleculares) del número de enlaces por átomo, y de las fuerzas intermoleculares.
Puedes ver este vídeo para entenderlo mejor.
Como puedes observar en tu tabla periódica, los gases nobles o inertes (grupo VIII) tienen 8 electrones en su ultima capa y se les llama inertes porque no se combinan con otras sustancias, no forman compuestos.
Lewis dedujo que esto último se debía a que la configuración de 8 electrones en la ultima capa de energía era la más estable para cualquier átomo.
Existen excepciones a esta regla. Los átomos que no cumplen la regla del octeto en algunos compuestos son: Carbono, Nitrógeno, Oxigeno y Azufre. En algunos casos estos elementos forman dobles enlaces y hasta triples el Carbono y el Nitrógeno.
martes, 8 de marzo de 2011
Oxidación reducción. Redox. Medio básico.
Medio básico
En medio básico se agregan iones hidróxilo (aniones) (OH−) y agua (H2O) a las semirreacciones para balancear la ecuación final.
Por ejemplo, tenemos la reacción entre el Permanganato de Potasio y el Sulfito de Sodio.
Ecuación sin balancear:
Separamos las semirreacciones en
- Oxidación:

- Reducción:
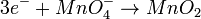
Agregamos la cantidad adecuada de Hidróxidos y Agua (las moléculas de agua se sitúan en donde hay mayor cantidad de oxígenos).
- Oxidación:

- Reducción:

Balanceamos la cantidad de electrones al igual que en el ejemplo anterior.
- Oxidación:

- Reducción:

Obtenemos:
- Oxidación:

- Reducción:

Como se puede ver, los electrones están balanceados, así que procedemos a sumar las dos semirreacciones, para obtener finalmente la ecuación balanceada.

 .
.- Fuente Wikipedia.
Oxidación reducción. Redox. Medio ácido.
Medio ácido
En medio ácido se agregan hidronios (cationes) (H+) y agua (H2O) a las semirreacciones para balancear la ecuación final.
Del lado de la ecuación que haga falta oxígeno se agregarán moléculas de agua, y del lado de la ecuación que hagan falta hidrógenos se agregarán hidronios.
Por ejemplo, cuando el Manganeso (II) reacciona con el Bismutato de Sodio.
Ecuación sin balancear:
- Oxidación :

- Reducción :

Ahora tenemos que agregar los hidronios y las moléculas de agua donde haga falta hidrógenos y donde haga falta oxígenos, respectivamente.
- Oxidación:

- Reducción:

Las reacciones se balancearán al momento de igualar la cantidad de electrones que intervienen en ambas semirreacciones. Esto se logrará multiplicando la reacción de una semirreación por el número de electrones de la otra semirreacción (y, de ser necesario, viceversa), de modo que la cantidad de electrones sea constante.
- Oxidación:
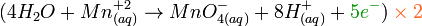
- Reducción:

Al final tendremos:
- Oxidación:

- Reducción:

Como se puede ver, los electrones están balanceados, así que procedemos a sumar las dos semirreacciones, para obtener finalmente la ecuación balanceada.

 .
.- Fuente: Wikipedia.
FORMAS DE REPRESENTAR MOLÉCULAS ORGÁNICAS.
En la química del carbono, es fácil encontrar diversos compuestos diferentes con la misma fórmula molecular. Para diferenciarlos, debemos s...

-
Cambios de estado progresivos : Son los cambios de estado cuando se aporta energía. Estos son: 1º- De estado de sólido a líquido . Se deno...
-
En un átomo, los electrones están girando alrededor del núcleo formando capas. En cada una de ellas, la energía que posee el electrón es dis...
-
La Estructura o diagrama de Lewis es una representación gráfica que muestra los enlaces entre los átomos de una molécula y los pares de elec...